烟酰胺腺嘌呤二核苷酸(nad)作为生物体内最重要的辅酶和核心代谢物,不仅广泛参与了能量代谢氧化还原反应,还是直接调控sirtuins、parp和cd38等重要酶活性的限制性底物,影响了表观遗传修饰、基因组完整性与信号转导过程。近来许多研究表明nad的水平常常伴随机体衰老而降低,而补充nad前体则可延缓衰老的进程。因此,在体nad水平的测定可帮助预测机体衰老进程和搜寻上调nad水平的抗衰老药物。然而,在体nad水平的测定无法通过传统生物化学分析方法实现,是本领域有待解决的重要技术挑战。
2020年3月19日,华东理工大学生物反应器工程国家重点实验室、药学院、光遗传学与合成生物学交叉学科研究中心赵玉政教授与杨弋教授合作在国际权威学术期刊developmental cell发表题为“illuminating nad metabolism in live cells and in vivo using a genetically encoded fluorescent sensor”的技术长文,报道一种nad代谢成像新技术,可原位、实时动态追踪细菌、哺乳动物细胞、斑马鱼、小鼠以及人源尿液干细胞等多种生物体内nad代谢水平。据悉,这也是该杂志近五年发表的国内首篇“technology article”。

在研究中,团队经过大量筛选和优化,获得一个高响应、高灵敏、大动态范围检测nad代谢的遗传编码荧光探针finad,并在细菌、酵母、哺乳动物细胞、斑马鱼和活体小鼠水平建立了前沿nad成像新技术。在生物体内,nad有三条合成途径,主要涉及烟酸(a)、烟酰胺(nam)、烟酰胺单核苷酸(nmn)和烟酰胺核糖(nr)四种前体。这些nad前体在医药食品和美容保健等领域有着广泛的应用,如na是治疗高血脂症的药物之一,nam是多种功能饮料和护肤品的添加成分,nmn和nr则是炙手可热的抗衰老新星,近来受到极大关注。利用finad,团队首次绘制了四种nad合成前体na、nam、nmn和nr在不同物种中调控nad代谢的可视化图谱,并对细菌、哺乳动物细胞、斑马鱼以及小鼠利用nad合成前体进行偏好性分析。研究发现,nmn和nr能显著提升细菌、哺乳动物体内nad水平,然而nam对哺乳动物更有效,却对细菌影响较小。nmn和nr已被多项研究用于延缓衰老及相关疾病,然而同为nad补救合成途径前体的nam功效甚微,这暗示肠道微生物菌群nad代谢可能与健康长寿存在某种联系。有趣的是,finad指示斑马鱼和其他几个物种相比,具有一套独特的nad合成代谢体系——nam-nampt轴介导的补救合成途径。相较于nam、nmn和nr,na无法在各种生物体内提升nad,但当补救合成途径受到抑制时,na介导的preiss-handler途径可被激活促进nad合成。通过筛选不同化合物,finad探针指示二甲双胍可增加胞内nad水平,这启示二甲双胍的多种神奇药效可能与提升nad水平有关,这将为探索二甲双胍作用机制提供新的思路。

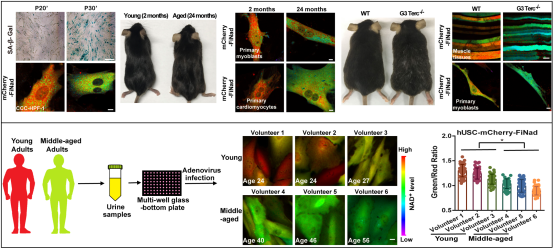
研究进一步发现,巨噬细胞激活过程中nad代谢发挥至关重要的作用,下调nad合成显著抑制巨噬细胞激活过程中糖酵解水平,炎症因子释放以及生物功能发挥。为了阐明衰老过程中nad的代谢情况,研究团队分别从经典的复制性衰老细胞、端粒酶缺失早衰小鼠以及自然性衰老小鼠模型入手,首次以可视化的高清图像,直观地展示了衰老过程中nad水平的衰退。尿检是一种常规的医学检测手段,从尿液样品中提取的人源尿液干细胞(husc)可部分反映人体的代谢状况。研究通过将finad探针导入不同年龄志愿者的husc细胞,清晰显示nad水平随年龄的增长而逐渐衰减。这一成果实现了一种无创评价人体衰老的全新尝试,使实验室技术和临床诊断无缝衔接,有望使科研成果快速转化应用到大众的医疗保健中,从而制定个性化的保健和诊疗策略。
烟酰胺腺嘌呤二核苷酸(nad/nadh)及其磷酸化形式nadp/ nadph,作为所有生物体内最重要的两个辅酶和核心代谢物,参与了众多的生理、病理学过程,也与许多疾病发生发展密切相关。近几年,围绕细胞代谢检测的瓶颈难题,杨弋教授、赵玉政教授合作开发了nadh探针frex、nad/nadh比率探针sonar、nadph探针inap等系列原创技术,并建立了“高通量”与“全景式”活细胞代谢监测分析方法,应用于候选药物快速筛选与临床样本即时检测,系列工作发表在2011 cell metabolism、2015 cell metabolism、2016 nature protocols、2017 nature methods、2018 nature protocols、2019 cell metabolism。随着新成员nad探针finad的加入,全面系统检测细胞内辅酶ⅰ、ⅱ的“四大金刚”(frex、sonar、inap和finad)已悉数到位。鉴于nad/nadh和nadp/ nadph在细胞代谢中的中心作用,对生物体内的分布及其代谢进行原位、实时动态的定量检测和成像,不仅为人们更好地理解物质与能量代谢的调节机制和代谢网络提供创新性的研究工具,也为临床样本的即时诊断与创新药物的筛选发现提供重要技术支撑,对人类生命健康具有重要意义。
我校的博士研究生邹叶君、王傲雪、黄立、呼庆勋,以及杭州师范大学的朱栩栋副研究员为本论文的共同第一作者,赵玉政、杨弋为通讯作者。这项工作得到哈佛大学医学院joseph loscalzo教授、暨南大学鞠振宇教授、同济大学附属东方医院王从容主任医师、华东理工大学朱麟勇教授、温州医科大学周永教授的大力支持帮助。研究工作得到国家自然科学基金、国家重点研发计划、中国医学科学院医学与健康科技创新工程、上海市科委、张江国家自主创新示范区专项发展基金等科研项目资助。
原文链接: